भारतीय शिक्षा में बदलाव
सरल आसवन प्रयोग क्या है?
सरल आसवन घटकों को उनके क्वथनांक में अंतर के आधार पर उनके द्रव मिश्रण से पृथक करता है। इस विधि में, पृथक किए जाने वाले मिश्रण को गर्म किया जाता है और फिर जल संघनक का उपयोग करके ठंडा किया जाता है। फिर संघनक नली के निकास से संघनित वाष्प को एकत्रित किया जाता है। उच्च वाष्प दाब वाले घटक का क्वथनांक निम्न होता है, इसलिए यह उच्च क्वथनांक वाले घटक से पहले वाष्पित और एकत्रित हो जाता है।
इस प्रकार, विभिन्न घटकों को विभिन्न क्वथनांकों पर एकत्रित किया जाता है। जब मिश्रण के घटकों के क्वथनांक में अंतर अत्यधिक (25°C से अधिक) होता है, तब यह विधि उनके पृथक्करण के लिए सबसे उपयुक्त है। संघनन के बाद प्राप्त द्रव को आसुत कहा जाता है और इसे एक बीकर या कोनिकल फ्लास्क में आसानी से एकत्रित किया जा सकता है।
सरल आसवन विधि का आरेख
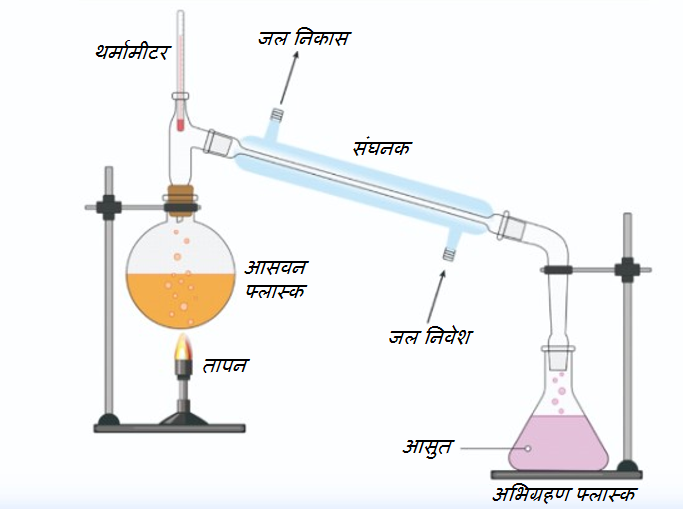
सरल आसवन
सरल आसवन की ऊपर दिखाई गई व्यवस्था में एक आसवन फ्लास्क होता है, जिसमें मिश्रण को उबालने के लिए रखा जाता है। एक संघनक, आसवन स्तंभ की भुजा से जुड़ा होता है, जो अलग-अलग क्वथनांकों पर घटकों को एकत्रित करने में सहायता करता है।
सरल आसवन के चरण कौन-कौन से हैं?
सरल आसवन में निम्नलिखित चरण शामिल हैं:
- आसवन फ्लास्क में मिश्रण को पृथक करने के लिए रखिए।
- कॉर्क में एक थर्मामीटर को जोड़िए और इसे आसवन फ्लास्क के अंदर रखिए।
- एक संघनक को आसवन फ्लास्क की पार्श्व भुजा से नीचे की ओर झुकाकर रखा जाता है। संघनक के निकास पर एक बीकर रखिए।
- मिश्रण को धीरे-धीरे गर्म करना शुरू कीजिए और जैसे ही पहला घटक उबलना शुरू होता है, थर्मामीटर पर तापमान का निरीक्षण कीजिए।
- निम्न वाष्प दाब वाला घटक पहले उबलता है, और जैसे ही वे संघनक तक पहुंचते हैं, इसकी वाष्प संघनित हो जाती है।
- संघनक वाष्प को ठंडा करता है, और आसुत को एकत्रित किया जाता है।
- जैसे-जैसे पहला घटक वाष्पित होता है, आसवन फ्लास्क में मिश्रण को अधिक से अधिक गर्म करने की आवश्यकता होती है, क्योंकि मिश्रण में अब उच्च क्वथनांक वाला घटक होता है।
- तापन अगले घटक को वाष्पित करना जारी रखता है।
- उस तापमान का निरीक्षण कीजिए, जिस पर दूसरा घटक उबलना शुरू कर देता है।
- वाष्प को संघनित करके एक अलग बीकर में एकत्रित किया जाता है।
आसवन के विभिन्न प्रकार क्या हैं?
नीचे आसवन के कई प्रकार दिए गए हैं:
- सरल आसवन: सरल आसवन, मिश्रण के घटकों को उनके क्वथनांक में सार्थक अंतर (25 °C से अधिक) के आधार पर पृथक करता है। मिश्रण को गर्म किया जाता है और घटक अलग-अलग तापमान पर उबलने के कारण पृथक हो जाते हैं।
- भाप आसवन: भाप आसवन में ऐसे मिश्रणों को पृथक करने की प्राथमिकता दी जाती है, जिनमें घटक ऊष्मा संवेदी होते हैं और सीधे गर्म करने पर अपघटित हो जाते हैं। भाप का उपयोग द्रव मिश्रण को गर्म करने के लिए किया जाता है।
- निर्वात आसवन: जब मिश्रण में उपस्थित घटकों का क्वथनांक बहुत अधिक होता है, तब निर्वात आसवन का उपयोग किया जाता है। आसवन फ्लास्क में एक निर्वात निर्मित किया जाता है, जो घटक के क्वथनांक को कम कर देता है, और इस प्रकार निम्न तापमान पर पृथक्करण प्राप्त होता है।
- प्रभाजी आसवन: जब मिश्रण के घटकों के क्वथनांक में अंतर 10 K-15 K का होता है, तब प्रभाजी आसवन का उपयोग किया जाता है। मिश्रण का पृथक्करण आसवन फ्लास्क से जुड़े “प्रभाजी स्तंभ” के उपयोग द्वारा होता है।
प्रभाजी आसवन क्या है?
प्रभाजी आसवन मिश्रणीय द्रवों को पृथक करने की एक विधि है। जब मिश्रण के घटकों के क्वथनांकों में अंतर 10 K -15 K का होता है, तब इसका उपयोग किया जाता है। जब घटकों के क्वथनांक एक दूसरे के निकट होते हैं, तो दोनों द्रवों की वाष्प साथ-साथ निर्मित होती है, और आसुत में दोनों घटकों की कुछ मात्रा उपस्थित होती है। इसलिए ऐसी स्थिति में, आसवन के लिए आसवन फ्लास्क से जुड़े एक प्रभाजी स्तंभ की आवश्यकता होती है। एक प्रभाजी स्तंभ में काँच के मोतियों या पत्थरों से भरी एक लंबी काँच की नली होती है, जो वाष्प के लिए अतिरिक्त शीतलन पृष्ठीय क्षेत्र प्रदान करती है।
जब द्रव मिश्रण को गर्म किया जाता है, तो दोनों द्रव वाष्पित हो जाते हैं, जिससे वाष्प का निर्माण होता है। उच्च वाष्प दाब वाला द्रव, प्रभाजी स्तंभ तक जाता है और काँच के मोतियों पर संघनित हो जाता है। द्रव की वाष्प, निम्न वाष्प दाब के साथ इस संघनन के दौरान मुक्त ऊर्जा को ग्रहण कर लेती है, और इसकी वाष्प, प्रभाजी स्तंभ में ऊपर पहुँच जाती है। साथ ही, बाद वाला द्रव, द्रव अवस्था में रहता है और आसवन फ्लास्क में वापस आ जाता है। इस प्रकार, निम्न क्वथनांक वाला द्रव पहले संघनक तक पहुँचता है और आसुत के रूप में एकत्रित कर लिया जाता है।
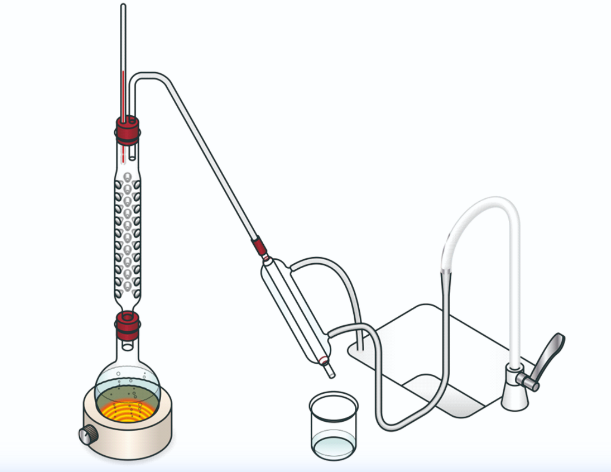
सरल आसवन और प्रभाजी आसवन के बीच क्या अंतर है?
विद्यार्थी नीचे दी गई सारणी से सरल और प्रभाजी आसवन के बीच अंतर ज्ञात कर सकते हैं।
| सरल आसवन | प्रभाजी आसवन |
|---|---|
| यह मिश्रणीय मिश्रण से उनके क्वथनांक में सार्थक अंतर वाले घटकों को पृथक करता है। | यह मिश्रणीय मिश्रण से लगभग समान क्वथनांक वाले घटकों को पृथक करता है। |
| द्रव को गर्म करने पर निर्मित वाष्प सीधे जल में संघनित हो जाती है। | निर्मित वाष्प को प्रभाजी स्तंभ के अंदर पहले संघनित और वाष्पित किया जाता है और फिर यह जल संघनक तक पहुँचती है। |
| उच्च वाष्प दाब वाले द्रवों को पहले एकत्रित किया जाता है, और फिर निम्न क्वथनांक वाले द्रवों को एकत्रित किया जाता है। | निम्न क्वथनांक वाले द्रव को पहले एकत्रित किया जाता है और फिर उच्च वाष्प दाब वाले द्रव संघनक तक पहुँचते हैं। |
| उदाहरण: सरल आसवन के उपयोग द्वारा ऐसीटोन (क्वथनांक 329K) और जल (क्वथनांक 373K) के मिश्रण को पृथक किया जा सकता है। | उदाहरण: ऐसीटोन (क्वथनांक 329K) और मेथेनॉल (क्वथनांक 337.7K) के मिश्रण को प्रभाजी आसवन का उपयोग करके पृथक किया जाता है। |
आसवन प्रक्रिया के अनुप्रयोग और उदाहरण:
आसवन प्रक्रिया के विभिन्न अनुप्रयोग हैं, जैसे कि:
- गैसोलीन का उत्पादन: अपरिष्कृत तेल के कई घटक ईंधन के रूप में अनुपयुक्त होते हैं और इसलिए अपरिष्कृत तेल को विभिन्न घटकों में पृथक करने के लिए आसवन बहुत उपयोगी होता है। यह आसवन के सबसे बड़े ज्ञात औद्योगिक अनुप्रयोगों में से एक है।
- जल का शोधन: विभिन्न हानिकारक खनिजों और अन्य अशुद्धियों को जल से निष्कासित किया जा सकता है। इसका उपयोग आसुत जल के उत्पादन जैसे कई औद्योगिक अनुप्रयोगों में किया जाता है।
- तेलों का पुनर्चक्रण: समय के साथ तेल का पुन: उपयोग उन्हें जल और अन्य अशुद्धियों से संदूषित कर सकता है इस तेल को प्रभाजी आसवन का उपयोग करके शोधित किया जा सकता है।
- अनिवार्य तेलों का संश्लेषण: फूलों का भाप आसवन अनिवार्य तेलों और जल आधारित आसुत के उत्पादन में सहायक होता है। इसका औद्योगिक रूप से उपयोग विभिन्न इत्रों के उत्पादन में किया जाता है।
- विभिन्न ऐल्कोहॉलिक पेय पदार्थों का उत्पादन: एथेनॉल उत्पादन के दौरान किण्वित पदार्थ को आसवन के उपयोग द्वारा सांद्रित और शोधित किया जा सकता है। आसवन के दौरान एथेनॉल की सुगंध और सांद्रता के आधार पर विभिन्न पेय पदार्थों को तैयार किया जा सकता है।
- समुद्रों में तेल के रिसाव का उपचार: प्रभाजी आसवन का उपयोग समुद्र में तेल के रिसाव के उपचार के लिए किया जाता है। यह रिसाव द्वारा फैले हुए तेल को विभिन्न उपयोगी अपरिष्कृत तेलों में पृथक करता है।
सरल प्रभाजी आसवन प्रयोग
प्रयोग का शीर्षक
सरल प्रभाजी आसवन प्रयोग
प्रयोग का विवरण
सरल आसवन दो मिश्रणीय द्रवों के मिश्रण को उनके क्वथनांक में अंतर के आधार पर पृथक करता है। आइए हम एक सरल आसवन प्रयोग करते हैं।
प्रयोग का उद्देश्य
सरल आसवन प्रक्रिया द्वारा दो मिश्रणीय द्रवों के मिश्रण को पृथक करना।
आवश्यक उपकरण और सामग्री
नीचे आवश्यक उपकरण दिए गए हैं:
- आसवन फ्लास्क
- प्रयोगशाला थर्मामीटर ( -10 °C से 110 °C)
- संघनक
- दो बीकर ( 250 मिली)
- त्रिपाद स्टैंड
- तार की जाली
- एकल छिद्रित कॉर्क
- बर्नर
- लोहे का स्टैंड
सामग्रियाँ
जल और ऐसीटोन का मिश्रण
प्रक्रिया
विद्यार्थी नीचे दिए गए चरणों के अनुसार प्रयोग कर सकते हैं।
- चरण 1: बर्नर के ऊपर त्रिपाद स्टैंड और उस पर तार की जाली रखिए।
- चरण 2: आसवन फ्लास्क को त्रिपाद स्टैंड पर रखा जाना चाहिए और लोहे के स्टैंड में कस दिया जाना चाहिए।
- चरण 3: अब एकल छिद्रित कॉर्क का उपयोग करके फ्लास्क को सील कर दें। द्रव को उबालने के दौरान तापमान को मापने के लिए कॉर्क के छिद्र में एक प्रयोगशाला थर्मामीटर डालिए।
- चरण 4: लोहे के स्टैंड से जुड़े एक संघनक में आसवन फ्लास्क की भुजा को डालें।
- चरण 5: संघनक के निवेश (इनलेट) और निकास (आउटलेट) को जल के पाइपों से ठीक से जोड़ा जाना चाहिए।
- चरण 6: संघनक के खुले सिरे के नीचे एक खाली बीकर रखिए।
- चरण 7: ऐसीटोन और जल के मिश्रण को धीरे-धीरे गर्म कीजिए और तापमान वृद्धि की सावधानीपूर्वक निगरानी कीजिए।
- चरण 8: उस तापमान को देखिए और नोट कीजिए जिस पर मिश्रण का पहला घटक आसवित होता है अर्थात वाष्प ठंडी हो जाती है और संघनक के दूसरे सिरे पर रखे एक बीकर में एकत्रित हो जाती है।
- चरण 9: गर्म करना जारी रखिए और प्रेक्षित कीजिए और उस तापमान को नोट कीजिए, जिस पर दूसरा घटक आसवित होता है।
सावधानियाँ
प्रयोग करने से पहले विद्यार्थियों को सावधानियों को ध्यानपूर्वक पढ़ना चाहिए।
- किसी भी गलत पाठ्यांक से बचने के लिए आसवन फ्लास्क की भुजा पर थर्मामीटर बल्ब होना चाहिए।
- जब तक एक विशेष घटक पूरी तरह से पृथक नहीं हो जाता है, तब तक तापन एकसमान रूप से किया जाना चाहिए।
- आसवन फ्लास्क को वाष्प को बाहर निकलने से रोकने के लिए कॉर्क का उपयोग करके कसकर बंद किया जाना चाहिए।
- संघनक को ठंडे जल के सतत प्रवाह की आपूर्ति की जानी चाहिए।
सरल आसवन प्रयोग पर अक्सर पूछे जाने वाले प्रश्न
विद्यार्थी नीचे दिए गए सरल आसवन प्रयोग से संबंधित अक्सर पूछे जाने वाले प्रश्नों को देख सकते हैं।
हम क्वथनांक को कैसे परिभाषित करते हैं?
वह तापमान जिस पर द्रव का वाष्प दाब, द्रव के क्षेत्रफल के आस-पास के बाह्य दाब के बराबर हो जाता है, उसे द्रव के क्वथनांक के रूप में जाना जाता है।
मेथेनॉल 64oC पर उबलता है और एथेनॉल 78oC पर उबलता हैं। इन दो घटकों के मिश्रण को पृथक करने के लिए उपयोग की जाने वाली सबसे अच्छी विधि कौन-सी है?
प्रभाजी आसवन
मेथेनॉल और एथेनॉल के क्वथनांक के बीच का अंतर 14 K है। मिश्रणीय द्रवों से बने मिश्रण, जिनके क्वथनांकों के बीच का अंतर 25 K से कम होता है, को प्रभाजी आसवन के उपयोग द्वारा पृथक किया जा सकता है। सरल आसवन का उपयोग उन द्रवों को पृथक करने के लिए किया जाता है, जिनके क्वथनांकों के बीच का अंतर 25 K से अधिक होता है।
जल 100oC पर उबलता है। जबकि एथेनॉल 78oC पर उबलता है। इनमें से किसमें प्रबल अंतरा-अणुक आकर्षण बल होता है?
जल
जल का क्वथनांक एथेनॉल की तुलना में उच्च होता है। यह इंगित करता है कि जल के अणु पर्याप्त रूप से निकट होते हैं और एक प्रबल अंतरा-अणुक आकर्षण बल द्वारा एक दूसरे से बंधित होते हैं। इसलिए, वाष्पन के दौरान अणुओं को पृथक करने के लिए जल को एथेनॉल की तुलना में अधिक ऊष्मा की आवश्यकता होती है।
आसवन फ्लास्क में पॉर्सिलेन (चीनी मिट्टी) के टुकड़ों का क्या उपयोग है?
आसवन फ्लास्क को गर्म करते समय विलयन वाष्पित हो जाता है। असमान रूप से गर्म करने के कारण विलयन को उच्छलन से रोकने के लिए आसवन फ्लास्क में पॉर्सिलेन के टुकड़ों को रखा जाता है।
क्वथन और वाष्पन के बीच क्या अंतर है?
वाष्पन एक प्राकृतिक प्रक्रिया है, जो तब होती है, जब दाब या ताप में वृद्धि के कारण द्रव, गैस में परिवर्तित हो जाता है। वाष्पन, बुलबलों का निर्माण नहीं करता है। क्वथन एक अप्राकृतिक प्रक्रिया है, जिसमें द्रव गर्म हो जाता है और द्रव के लगातार गर्म होने के कारण यह वाष्पित हो जाता है। क्वथन, गर्म करने के दौरान लगातार बुलबलों का निर्माण करता है।